#آزمون سمیت سیستمیک حاد داخل وریدی#آزمون سمیت حاد سیستمیک داخل وریدی#آزمون سمیت حاد داخل وریدی#آزمون سیستمیک حاد داخل وریدی#Hcl,k sldj sdsjld; phn nhog ,vdnd#آزمون سمیت سیستمیک حاد درون وریدی#آزمون سمیت حاد سیستمیک درون وریدی#آزمون سمیت حاد درون وریدی#آزمون سیستمیک حاد درون وریدی#acute intravascular toxicity tests#تست سمیت سیستمیک حاد وریدی#آزمون سمیت حاد وریدی#تست سمیت سیستمیک حاد داخل وریدی آزمون سمیت سیستمیک حاد داخل وریدی – دوز ثابت | Acute Intravenous Toxicity – Fixed Dose آزمون سمیت سیستمیک حاد داخل وریدی، جهت ارزیابی پتانسیل سمیت حاد و محاسبه دوز متوسط کشنده (LD50 ) محدوده وسیعی از مواد، محصولات پزشکی و دارو های تزریقی که به شکل درون رگی تجویز می شوند، در بازه ۱۴ روزه پس از تزریق به حیوانات بکار می رود. آزمون سمیت حاد یک تخمینی کلی از ماهیت سمی نمونه آزمایشی را مشخص می کند و همچنین نتایج حاصل از آن جهت تعیین دوز شروع سایر آزمون های سیستمیک مانند آزمون سمیت سیستمیک تحت حاد ، آزمون سمیت سیستمیک تحت مزمن و آزمون سمیت سیستمیک مزمن استفاده خواهد شد.
#آزمون سمیت سیستمیک حاد داخل رگی#آزمون سمیت حاد سیستمیک داخل رگی#آزمون سمیت حاد داخل رگی#آزمون سیستمیک حاد داخل رگی#acute intravascular systemic toxicity tests#آزمون سمیت سیستمیک حاد درون رگی#آزمون سمیت حاد سیستمیک درون رگی#آزمون سمیت حاد درون رگی#آزمون سیستمیک حاد درون رگی#Hcl,k sldj phn nhog ,vdnd#تست سمیت حاد داخل وریدی روش کار در مجموعه آزمایشگاه های سنجش و پایش کیاژن فارما، آزمون سمیت سیستمیک حاد – دوز ثابت، بر روی موش نژاد سوری (NMRI) و یا رت آزمایشگاهی به صورت زیر انجام می شود:
پیش از شروع کار، ابتدا مطالعات نظری و گذشته نگر از نظر موارد زیر بر روی ماده آزمایشی و یا محصولات مشابه انجام خواهد شد تا اطلاعات کلی در مورد سمیت ماده آزمایشی و دوز شروع آزمون حاصل شود. کلیه موارد بر اساس مولفه ها و معیارهای استاندارد ISO 10993-1 انتخاب و ارزیابی خواهند شد.
برگه پرسشنامه پر شده توسط متقاضی در خصوص ویژگی های محصول (intended use/device characteristics) فرآیند مدیریت ریسک مواد (risk management process) تحلیل ریسک مواد تشکیل دهنده محصول (risk analysis) شناسایی خطرات بیولوژیک محصول (biological hazard identification) ارزیابی در معرض قرار گیری محصول (exposure assessment) کنترل ریسک مواد تشکیل دهنده محصول (risk control) اطلاعات پس از تولید محصول (post-production information)
مطالعات نظری پیش از شروع تستهای درونتنی، یک فعالیت علمی و بسیار مهم است که جهت توجیه و برنامه ریزی صحیح جهت ارزیابی خطرات بیولوژیکی یک ماده / وسیله و همچنین جهت کسب اطلاعات ضروری برای رعایت اصول اخلاقی کار با حیوانات آزمایشی (اصول سه گانه) و انتخاب روش مناسب جهت آماده سازی نمونه باید انجام شود.
چنین مطالعاتی مشخص می کند که آیا داده های موجود، برای نشان دادن ایمنی بیولوژیکی ماده / وسیله / دستگاه پزشکی مورد نظر، بدون نیاز به انجام آزمون های داخل بدنی، کافی است یا خیر؟! اگر پس از مطالعات تئوری، داده ها از نظر سطوح ایمن مواجهه بالینی، قابل قبول ارزیابی شد و یا اگر داده های سم شناسی حاکی از امکان انجام آزمون درون بدن حیوانات باشد، بخش حیوانی کیاژن فارما اقدام به انجام تست داخل تنی خواهد کرد.
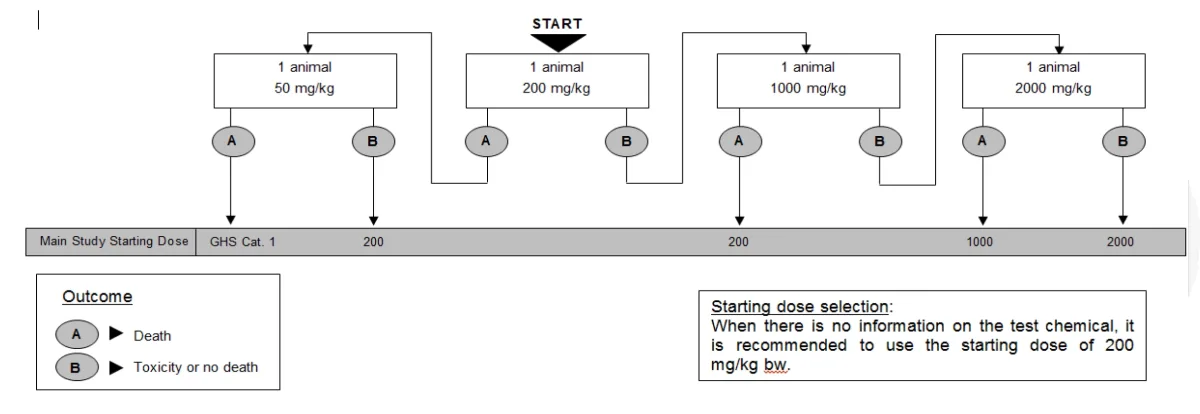
#آزمون سمیت سیستمیک حاد داخل وریدی#آزمون سمیت حاد سیستمیک داخل وریدی#آزمون سمیت حاد داخل وریدی#آزمون سیستمیک حاد داخل وریدی#Hcl,k sldj sdsjld; phn nhog ,vdnd#آزمون سمیت سیستمیک حاد درون وریدی#آزمون سمیت حاد سیستمیک درون وریدی#آزمون سمیت حاد درون وریدی#آزمون سیستمیک حاد درون وریدی#acute intravascular toxicity tests#تست سمیت سیستمیک حاد وریدی#آزمون سمیت حاد وریدی#تست سمیت سیستمیک حاد داخل وریدی آزمون مقدماتی | Pilot Study در بخش حیوانی مجموعه آزمایشگاه های سنجش و پایش کیاژن فارما، هدف از انجام تست مقدماتی، مشخص کردن دوز مناسب آزمایه جهت شروع تست اصلی است. هنگامیکه بر اساس مطالعات نظری انجام شده پیش از شروع تست، اطلاعات کافی در مورد نمونه وجود ندارد، یک تست مقدماتی مطابق روش زیر جهت یافتن دوز شروع و با استفاده از تعداد حداقلی از حیوانات انجام می شود:
موش های سوری (NMRI) ۶ تا ۸ هفته و با میانگین وزن ۲۰ تا ۳۰ گرم جهت انجام آزمون آماده خواهند شد.
حیوانات به صورت مرحله ای تحت تیمار با غلظت های ثابت ۵۰، ۲۰۰، ۱۰۰۰ و ۲۰۰۰ میلی گرم به ازای هر کیلوگرم وزن بدن حیوانات و بر اساس فلوچارت زیر قرار خواهند گرفت و از نظر علائم سمیت بررسی خواهند شد، سپس دوز مناسب آزمایه جهت دوز شروع آزمون اصلی در انتخاب خواهد شد.
#آزمون سمیت سیستمیک حاد داخل رگی#آزمون سمیت حاد سیستمیک داخل رگی#آزمون سمیت حاد داخل رگی#آزمون سیستمیک حاد داخل رگی#acute intravascular systemic toxicity tests#آزمون سمیت سیستمیک حاد درون رگی#آزمون سمیت حاد سیستمیک درون رگی#آزمون سمیت حاد درون رگی#آزمون سیستمیک حاد درون رگی#Hcl,k sldj phn nhog ,vdnd#تست سمیت حاد داخل وریدی #آزمون سمیت سیستمیک حاد داخل وریدی#آزمون سمیت حاد سیستمیک داخل وریدی#آزمون سمیت حاد داخل وریدی#آزمون سیستمیک حاد داخل وریدی#Hcl,k sldj sdsjld; phn nhog ,vdnd#آزمون سمیت سیستمیک حاد درون وریدی#آزمون سمیت حاد سیستمیک درون وریدی#آزمون سمیت حاد درون وریدی#آزمون سیستمیک حاد درون وریدی#acute intravascular toxicity tests#تست سمیت سیستمیک حاد وریدی#آزمون سمیت حاد وریدی#تست سمیت سیستمیک حاد داخل وریدی آزمون اصلی | Main Study
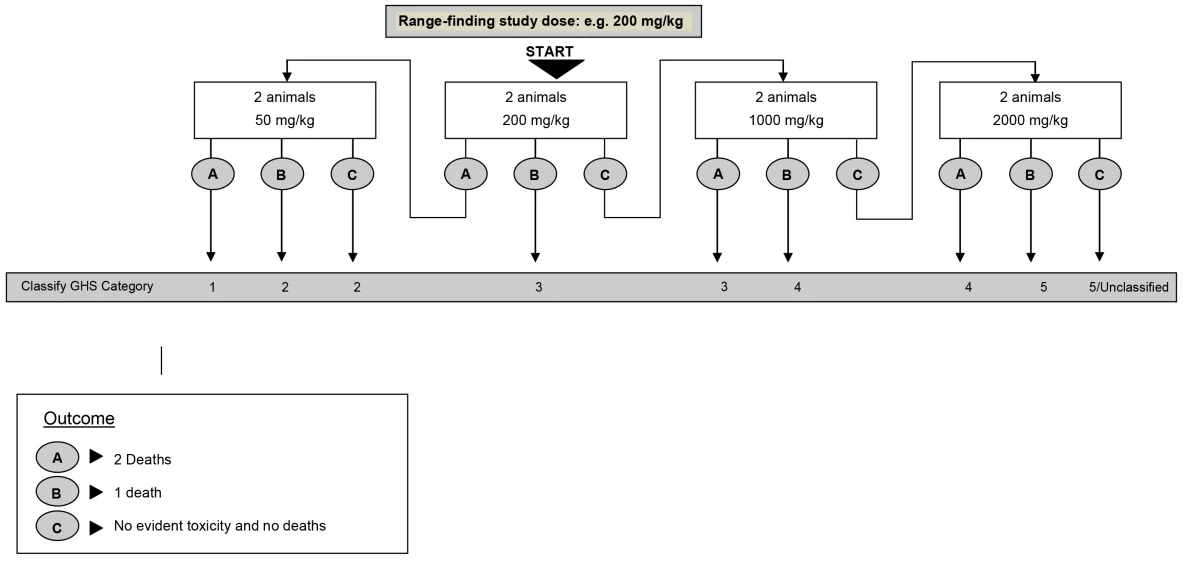
در آزمون اصلی، حیوانات بر اساس فلوچارت های زیر و به صورت مرحله ای تا رسیدن به هدف آزمون، تحت تیمار با دوز های آزمایه قرار خواهند گرفت.
در نهایت دوز سمی ماده آزمایشی و دسته GHS آن گزارش خواهد شد.
طول مدت مشاهدات حیوانات تست، از زمان شروع تا پایان آزمون، حداقل به مدت ۱۴ روز است.
در پایان آزمون، کلیه حیوانات بر اساس موازین اخلاقی، معدوم و کالبدگشایی شده و اندام های داخلی بدن مورد ارزیابی دقیق ماکروسکوپی و میکروسکوپی (در صورت لزوم) قرار خواهد گرفت.
#آزمون سمیت سیستمیک حاد داخل رگی#آزمون سمیت حاد سیستمیک داخل رگی#آزمون سمیت حاد داخل رگی#آزمون سیستمیک حاد داخل رگی#acute intravascular systemic toxicity tests#آزمون سمیت سیستمیک حاد درون رگی#آزمون سمیت حاد سیستمیک درون رگی#آزمون سمیت حاد درون رگی#آزمون سیستمیک حاد درون رگی#Hcl,k sldj phn nhog ,vdnd#تست سمیت حاد داخل وریدی استاندارد های زیست سازگاری | References ISO 10993-1: Biological Evaluation of Medical Devices – Evaluation and testing within a risk management process.
ISO 10993-2: Biological Evaluation of Medical Devices – Animal welfare requirements.
ISO 10993-3: Biological Evaluation of Medical Devices – Tests for genotoxicity, carcinogenicity and reproductive toxicity.
ISO 10993-4: Biological Evaluation of Medical Devices – Selection of tests for interactions with blood.
ISO 10993-5: Biological Evaluation of Medical Devices – Tests for in vitro cytotoxicity.
ISO 10993-6: Biological Evaluation of Medical Devices – Tests for local effects after implantation.
ISO 10993-7: Biological Evaluation of Medical Devices – Ethylene oxide sterilization residuals.
ISO 10993-8: Biological Evaluation of Medical Devices – Selection and qualification of reference materials for biological tests.
ISO 10993-9: Biological Evaluation of Medical Devices – Framework for identification and quantification of potential degradation products.
ISO 10993-10: Biological Evaluation of Medical Devices – Tests for skin sensitization.
ISO 10993-11: Biological Evaluation of Medical Devices – Tests for systemic toxicity.
ISO 10993-12: Biological Evaluation of Medical Devices – Sample preparation and reference materials.
ISO 10993-13: Biological Evaluation of Medical Devices – Identification and quantification of degradation products from polymeric medical devices.
ISO 10993-14: Biological Evaluation of Medical Devices – Identification and quantification of degradation products from ceramics.
ISO 10993-15: Biological Evaluation of Medical Devices – Identification and quantification of degradation products from metals and alloys.
ISO 10993-16: Biological Evaluation of Medical Devices – Toxicokinetic study design for degradation products and leachables.
ISO 10993-17: Biological Evaluation of Medical Devices – Toxicological risk assessment of medical device constituents.
ISO 10993-18: Biological Evaluation of Medical Devices – Chemical characterization of medical device materials within a risk management process.
ISO 10993-19: Biological Evaluation of Medical Devices – Physico-chemical, morphological and topographical characterization of materials.
ISO 10993-20: Biological Evaluation of Medical Devices – Principles and methods for immunotoxicology testing of medical devices.
ISO 10993-22: Biological Evaluation of Medical Devices – Guidance on nanomaterials.
ISO 10993-23: Biological Evaluation of Medical Devices – Tests for irritation.
OECD Test No. 401: Guidelines for the Testing of Chemicals – Acute Oral Toxicity.
OECD Test No. 402: Guidelines for the Testing of Chemicals – Acute Dermal Toxicity.
OECD Test No. 403: Guidelines for the Testing of Chemicals – Acute Inhalation Toxicity.
OECD Test No. 404: Guidelines for the Testing of Chemicals – Acute Dermal Irritation/Corrosion.
OECD Test No. 405: Guidelines for the Testing of Chemicals – Acute Eye Irritation/Corrosion.
OECD Test No. 406: Guidelines for the Testing of Chemicals – Skin Sensitisation.
OECD Test No. 407: Guidelines for the Testing of Chemicals – Repeated Dose 28-day Oral Toxicity Study in Rodents.
OECD Test No. 408: Guidelines for the Testing of Chemicals – Repeated Dose 90-Day Oral Toxicity Study in Rodents.
OECD Test No. 409: Guidelines for the Testing of Chemicals – Repeated Dose 90-Day Oral Toxicity Study in Non-Rodents.
OECD Test No. 410: Guidelines for the Testing of Chemicals – Repeated Dose Dermal Toxicity: 21/28-day Study.
OECD Test No. 411: Guidelines for the Testing of Chemicals – Subchronic Dermal Toxicity: 90-day Study.
OECD Test No. 412: Guidelines for the Testing of Chemicals – Subacute Inhalation Toxicity: 28-Day Study.
OECD Test No. 413: Guidelines for the Testing of Chemicals – Subchronic Inhalation Toxicity: 90-day Study.
OECD Test No. 414: Guidelines for the Testing of Chemicals – Prenatal Developmental Toxicity Study.
OECD Test No. 415: Guidelines for the Testing of Chemicals – One-Generation Reproduction Toxicity Study.
OECD Test No. 416: Guidelines for the Testing of Chemicals – Two-Generation Reproduction Toxicity.
OECD Test No. 417: Guidelines for the Testing of Chemicals – Toxicokinetics.
OECD Test No. 418: Guidelines for the Testing of Chemicals – Delayed Neurotoxicity of Organophosphorus Substances Following Acute Exposure.
OECD Test No. 419: Guidelines for the Testing of Chemicals – Delayed Neurotoxicity of Organophosphorus Substances: 28-day Repeated Dose Study.
OECD Test No. 420: Guidelines for the Testing of Chemicals – Acute Oral Toxicity – Fixed Dose Procedure.
OECD Test No. 421: Guidelines for the Testing of Chemicals – Reproduction/Developmental Toxicity Screening Test.
OECD Test No. 422: Guidelines for the Testing of Chemicals – Combined Repeated Dose Toxicity Study with the Reproduction/Developmental Toxicity Screening Test.
OECD Test No. 423: Guidelines for the Testing of Chemicals – Acute Oral toxicity – Acute Toxic Class Method.
OECD Test No. 424: Guidelines for the Testing of Chemicals – Neurotoxicity Study in Rodents.
OECD Test No. 425: Guidelines for the Testing of Chemicals – Acute Oral Toxicity: Up-and-Down Procedure.
OECD Test No. 426: Guidelines for the Testing of Chemicals – Developmental Neurotoxicity Study.
OECD Test No. 427: Guidelines for the Testing of Chemicals – Skin Absorption: In Vivo Method.
OECD Test No. 428: Guidelines for the Testing of Chemicals – Skin Absorption: In Vitro Method.
OECD Test No. 429: Guidelines for the Testing of Chemicals – Skin Sensitisation.
OECD Test No. 430: Guidelines for the Testing of Chemicals – In Vitro Skin Corrosion: Transcutaneous Electrical Resistance Test Method (TER).
OECD Test No. 431: Guidelines for the Testing of Chemicals – In vitro skin corrosion: reconstructed human epidermis (RHE) test method.
OECD Test No. 432: Guidelines for the Testing of Chemicals – In Vitro 3T3 NRU Phototoxicity Test.
OECD Test No. 433: Guidelines for the Testing of Chemicals – Acute Inhalation Toxicity: Fixed Concentration Procedure.
OECD Test No. 434: Guidelines for the Testing of Chemicals – Acute Dermal Toxicity – Fixed Dose Procedure.
OECD Test No. 435: Guidelines for the Testing of Chemicals – In Vitro Membrane Barrier Test Method for Skin Corrosion.
OECD Test No. 436: Guidelines for the Testing of Chemicals – Acute Inhalation Toxicity – Acute Toxic Class Method.
OECD Test No. 437: Guidelines for the Testing of Chemicals – Bovine Corneal Opacity and Permeability Test Method for Identifying i) Chemicals Inducing Serious Eye Damage and ii) Chemicals Not Requiring Classification for Eye Irritation or Serious Eye Damage.
OECD Test No. 438: Isolated Chicken Eye Test Method for Identifying i) Chemicals Inducing Serious Eye Damage and ii) Chemicals Not Requiring Classification for Eye Irritation or Serious Eye Damage.
OECD Test No. 439: Guidelines for the Testing of Chemicals – In Vitro Skin Irritation: Reconstructed Human Epidermis Test Method.
OECD Test No. 440: Guidelines for the Testing of Chemicals – Uterotrophic Bioassay in Rodents.
OECD Test No. 441: Guidelines for the Testing of Chemicals – Hershberger Bioassay in Rats.
OECD Test No. 442A: Guidelines for the Testing of Chemicals – Skin Sensitization – Local Lymph Node Assay: DA.
OECD Test No. 442B: Guidelines for the Testing of Chemicals – Skin Sensitization – Local Lymph Node Assay: BrdU-ELISA or –FCM.
OECD Test No. 442C: Guidelines for the Testing of Chemicals – In Chemico Skin Sensitisation – Assays addressing the Adverse Outcome Pathway key event on covalent binding to proteins.
OECD Test No. 442D: Guidelines for the Testing of Chemicals – In Vitro Skin Sensitisation – ARE-Nrf2 Luciferase Test Method.
OECD Test No. 442E: Guidelines for the Testing of Chemicals – 442E: In Vitro Skin Sensitisation – In Vitro Skin Sensitisation assays addressing the Key Event on activation of dendritic cells on the Adverse Outcome Pathway for Skin Sensitisation.
OECD Test No. 443: Guidelines for the Testing of Chemicals – Extended One-Generation Reproductive Toxicity Study.
OECD Test No. 451: Guidelines for the Testing of Chemicals – Carcinogenicity Studies.
OECD Test No. 452: Guidelines for the Testing of Chemicals – Chronic Toxicity Studies.
OECD Test No. 453: Guidelines for the Testing of Chemicals – Combined Chronic Toxicity/Carcinogenicity Studies.
OECD Test No. 455: Guidelines for the Testing of Chemicals – Performance-Based Test Guideline for Stably Transfected Transactivation In Vitro Assays to Detect Estrogen Receptor Agonists and Antagonists.
OECD Test No. 456: Guidelines for the Testing of Chemicals – H295R Steroidogenesis Assay.
OECD Test No. 457: Guidelines for the Testing of Chemicals – BG1Luc Estrogen Receptor Transactivation Test Method for Identifying Estrogen Receptor Agonists and Antagonists.
OECD Test No. 458: Guidelines for the Testing of Chemicals – Stably Transfected Human Androgen Receptor Transcriptional Activation Assay for Detection of Androgenic Agonist and Antagonist Activity of Chemicals.
OECD Test No. 460: Guidelines for the Testing of Chemicals – Fluorescein Leakage Test Method for Identifying Ocular Corrosives and Severe Irritants.
OECD Test No. 471: Guidelines for the Testing of Chemicals – Bacterial Reverse Mutation Test.
OECD Test No. 473: Guidelines for the Testing of Chemicals – In Vitro Mammalian Chromosomal Aberration Test.
OECD Test No. 474: Guidelines for the Testing of Chemicals – Mammalian Erythrocyte Micronucleus Test.
OECD Test No. 475: Guidelines for the Testing of Chemicals – Mammalian Bone Marrow Chromosomal Aberration Test.
OECD Test No. 476: Guidelines for the Testing of Chemicals – In Vitro Mammalian Cell Gene Mutation Tests using the Hprt and xprt genes.
OECD Test No. 477: Guidelines for the Testing of Chemicals – Genetic Toxicology: Sex-Linked Recessive Lethal Test in Drosophila melanogaster.
OECD Test No. 478: Guidelines for the Testing of Chemicals – Rodent Dominant Lethal Test.
OECD Test No. 479: Guidelines for the Testing of Chemicals – Genetic Toxicology: In vitro Sister Chromatid Exchange Assay in Mammalian Cells.
OECD Test No. 480: Guidelines for the Testing of Chemicals – Genetic Toxicology: Saccharomyces cerevisiae, Gene Mutation Assay.
OECD Test No. 481: Guidelines for the Testing of Chemicals – Genetic Toxicology: Saacharomyces cerevisiae, Miotic Recombination Assay.
OECD Test No. 482: Guidelines for the Testing of Chemicals – Genetic Toxicology: DNA Damage and Repair, Unscheduled DNA Synthesis in Mammalian Cells in vitro.
OECD Test No. 483: Guidelines for the Testing of Chemicals – Mammalian Spermatogonial Chromosomal Aberration Test.
OECD Test No. 484: Guidelines for the Testing of Chemicals – Genetic Toxicology: Mouse Spot Test.
OECD Test No. 485: Guidelines for the Testing of Chemicals – Genetic toxicology, Mouse Heritable Translocation Assay.
OECD Test No. 486: Guidelines for the Testing of Chemicals – Unscheduled DNA Synthesis (UDS) Test with Mammalian Liver Cells in vivo.
OECD Test No. 487: Guidelines for the Testing of Chemicals – In Vitro Mammalian Cell Micronucleus Test.
OECD Test No. 488: Guidelines for the Testing of Chemicals – Transgenic Rodent Somatic and Germ Cell Gene Mutation Assays.
OECD Test No. 489: Guidelines for the Testing of Chemicals – In Vivo Mammalian Alkaline Comet Assay.
OECD Test No. 490: Guidelines for the Testing of Chemicals – In Vitro Mammalian Cell Gene Mutation Tests Using the Thymidine Kinase Gene.
OECD Test No. 491: Guidelines for the Testing of Chemicals – Short Time Exposure In Vitro Test Method for Identifying i) Chemicals Inducing Serious Eye Damage and ii) Chemicals Not Requiring Classification for Eye Irritation or Serious Eye Damage.
OECD Test No. 492: Guidelines for the Testing of Chemicals – Reconstructed human Cornea-like Epithelium (RhCE) test method for identifying chemicals not requiring classification and labelling for eye irritation or serious eye damage.
OECD Test No. 493: Guidelines for the Testing of Chemicals – Performance-Based Test Guideline for Human Recombinant Estrogen Receptor (hrER) In Vitro Assays to Detect Chemicals with ER Binding Affinity.
OECD Test No. 494: Guidelines for the Testing of Chemicals – Vitrigel-Eye Irritancy Test Method for Identifying Chemicals Not Requiring Classification and Labelling for Eye Irritation or Serious Eye Damage.
OECD Test No. 495: Guidelines for the Testing of Chemicals – Ros (Reactive Oxygen Species) Assay for Photoreactivity.
OECD Test No. 496: Guidelines for the Testing of Chemicals – In vitro Macromolecular Test Method for Identifying Chemicals Inducing Serious Eye Damage and Chemicals Not Requiring Classification for Eye Irritation or Serious Eye Damage.
OECD Test No. 497: Guidelines for the Testing of Chemicals – Defined Approaches on Skin Sensitisation.
OECD Test No. 498: Guidelines for the Testing of Chemicals – In vitro Phototoxicity – Reconstructed Human Epidermis Phototoxicity test method.
OECD Test No. 19: Guidance Document on the Recognition, Assessment and Use of Clinical Signs as Humane Endpoints for Experimental Animals Used in Safety Evaluation. Environmental Health and Safety Monograph Series on Testing and Assessment.
#آزمون سمیت سیستمیک حاد داخل وریدی#آزمون سمیت حاد سیستمیک داخل وریدی#آزمون سمیت حاد داخل وریدی#آزمون سیستمیک حاد داخل وریدی#Hcl,k sldj sdsjld; phn nhog ,vdnd#آزمون سمیت سیستمیک حاد درون وریدی#آزمون سمیت حاد سیستمیک درون وریدی#آزمون سمیت حاد درون وریدی#آزمون سیستمیک حاد درون وریدی#acute intravascular toxicity tests#تست سمیت سیستمیک حاد وریدی#آزمون سمیت حاد وریدی#تست سمیت سیستمیک حاد داخل وریدی #آزمون سمیت سیستمیک حاد داخل رگی#آزمون سمیت حاد سیستمیک داخل رگی#آزمون سمیت حاد داخل رگی#آزمون سیستمیک حاد داخل رگی#acute intravascular systemic toxicity tests#آزمون سمیت سیستمیک حاد درون رگی#آزمون سمیت حاد سیستمیک درون رگی#آزمون سمیت حاد درون رگی#آزمون سیستمیک حاد درون رگی#Hcl,k sldj phn nhog ,vdnd#تست سمیت حاد داخل وریدی #آزمایشگاه همکار سازمان ملی استاندارد #آزمایشگاه همکار سازمان غذا و دارو#آزمایشگاه همکار اداره کل تجهیزات پزشکی#آزمایشگاه سنجش و پایش کیاژن فارما#آزمایشگاه کیاژن فارما#آزمایشگاه کنترل کیفی کیاژن فارما#تعرفه آزمون های زیست سازگاری#قیمت آزمون های زیست سازگاری#قیمت آزمون های سم شناسی#تعرفه آزمون های سم شناسی #آزمون های کالای وارداتی#آزمون های کالای صادراتی#آزمون های تولیدات دارویی#همکار شرکت های دارویی #Kiagenpharma# Kiagen# اصلاح و نباتات #آزمون های تخصصی گمرکی#آزمون های گمرکی 









دیدگاهها
هیچ دیدگاهی برای این خدمت نوشته نشده است.